



Menganalisis dan menjelaskan konsep reaksi reduksi dan oksidasi, perubahan bilangan biloks, dan membandingkan hasil percobaan berdasarkan potensial elektron standar.
Reaksi Redoks adalah suatu reaksi kimia dimana terjadi pemindahan elektron dari satu reaktan ke reaktan yang lainnya.
Reaksi redoks spontan adalah reaksi yang berlangsung dengan sendirinya dan disertai pembebasan energi berupa panas yang ditandai dengan perubahan suhu.
Terjadi apabila harga E sel negatif. Suatu reaksi kimia (termasuk reaksi redoks) yang tidak spontan tidak akan terjadi dengan sendirinya.
Bilangan oksidasi adalah suatu bilangan yang dimiliki oleh suatu unsur berdasarkan elektron valensi dari unsur tersebut. Elektron valensi ini dapat digunakan atau ditarik oleh unsur lain dengan elektronegativitas yang lebih besar. Unsur bebas memiliki bilangan oksidasi (biloks) = 0.
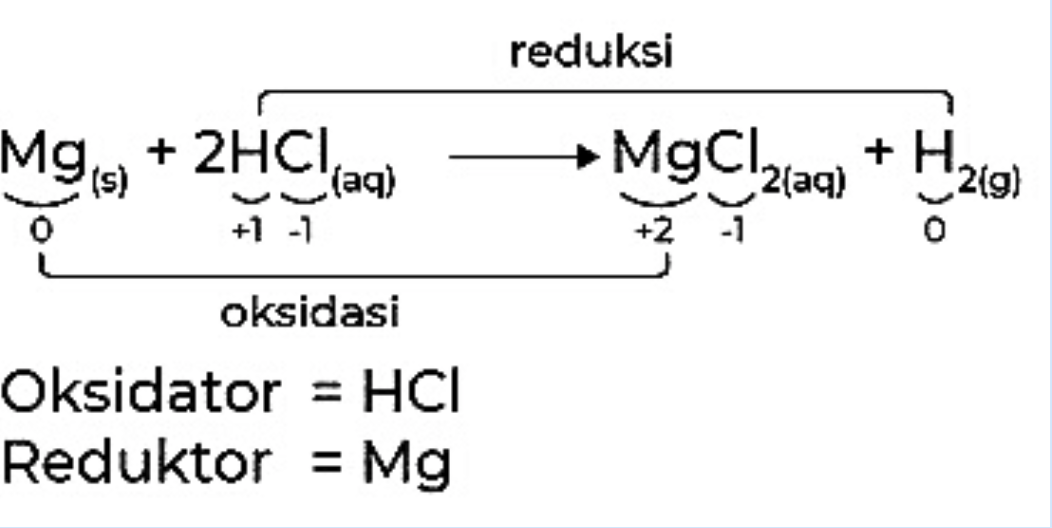
Oksidator adalah zat yang mengalami reduksi dalam suatu reaksi kimia, yaitu zat yang menyebabkan zat lain mengalami oksidasi.
Reduktor adalah zat yang mengalami oksidasi dalam suatu reaksi kimia, yaitu zat yang menyebabkan zat lain mengalami reduksi.
Reaksi oksidasi adalah reaksi di mana terjadi peningkatan bilangan oksidasi pada suatu unsur dan kehilangan elektron.
Reaksi reduksi adalah reaksi di mana terjadi penurunan bilangan oksidasi pada suatu unsur dan penambahan elektron.
Elektrode yang lebih mudah mengalami reduksi dibandingkan elektrode hidrogen (H2) memiliki tanda positif (E sel = +). Sebaliknya, elektrode yang lebih mudah mengalami oksidasi dan lebih sulit mengalami reduksi dibandingkan elektrode hidrogen (H2) memiliki tanda negatif (E sel = -).
Potensial elektrode suatu unsur yang mengalami reaksi redoks akan bernilai sama, namun tanda potensialnya akan berbeda pada reaksi oksidasi dan reduksi.
Untuk Magnesium (Mg):