



Siswa mampu memahami konsep kesetimbangan kimia dengan benar melalui praktikum. Siswa mampu mengaplikasikan hukum kesetimbangan kimia melalui dengan menggunakan perhitungan matematis dengan akurat. Siswa mampu mengidentifikasi faktor-faktor yang memengaruhi kesetimbangan kimia dengan tepat melalui eksperimen dan observasi yang dilakukan. Siswa mampu menghubungkan konsep kesetimbangan kimia dengan kehidupan sehari-hari melalui studi kasus yang diberikan dengan tepat. Siswa mampu menjelaskan arti dan signifikansi konstanta kesetimbangan (K) dengan baik melalui pemahaman yang mendalam tentang hubungannya dengan konsentrasi relatif reaktan dan produk dalam suatu reaksi kimia. Siswa mampu memprediksi dan menentukan arah pergeseran kesetimbangan melalui analisis efek perubahan konsentrasi, tekanan, atau suhu terhadap posisi kesetimbangan dengan benar. Siswa mampu menerapkan prinsip Le Chatelier secara efektif dalam menganalisis respons suatu reaksi kesetimbangan terhadap perubahan kondisi eksternalnya.
Reaksi kimia adalah peristiwa perubahan kimia dari zat-zat yang bereaksi (reaktan) menjadi zat-zat hasil reaksi (produk). Pada reaksi kimia selalu dihasilkan zat-zat yang baru dengan sifat-sifat yang baru pula. Reaksi kimia dapat dibedakan menjadi 2, yaitu reaksi reversible dan reaksi irreversible.
Reaksi reversible adalah reaksi dua arah (bolak-balik). Untuk jenis reaksi ini, hasil reaksi dapat kembali membentuk reaktan.
Contoh: Reaksi pembuatan gas ammonia dengan proses Haber Bosch
N2(g) + 3H2(g) ↔ 2NH3(g)
Reaksi irreversible adalah reaksi satu arah (tidak dapat balik), di mana untuk reaksi ini, hasil reaksi tidak dapat kembali membentuk reaktan.
Contoh: Reaksi antara larutan Natrium Hidroksida dengan HCl menghasilkan larutan NaCl
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l)
Pada reaksi reversible yang terjadi pada sistem tertutup (tidak ada perpindahan materi), kesetimbangan akan tercapai jika laju reaksi ke arah kanan sama dengan laju reaksi ke arah kiri. Pada kondisi tersebut, tidak ada perubahan yang teramati secara makroskopis. Konsentrasi reaktan seolah-olah tidak berubah atau tetap. Namun secara mikroskopis, reaksi terus berlangsung bolak-balik. Kesetimbangan seperti ini disebut sebagai kesetimbangan dinamis, yaitu proses reaksi bolak-balik yang lajunya sama untuk kedua arah.
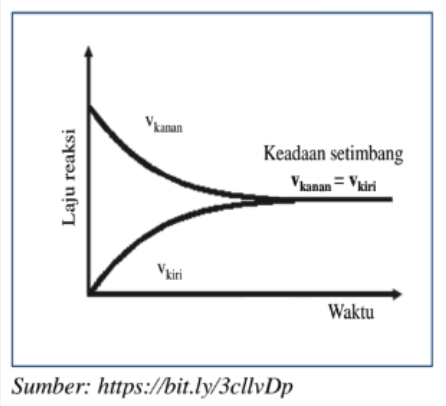
Tekanan adalah laju reaksi ke arah kanan (reaksi maju) sedangkan Vkiri adalah laju ke arah kiri (reaksi balik).
Tetapan kesetimbangan konsentrasi (Kc) adalah perbandingan hasil kali konsentrasi produk yang dipangkatkan koefisiennya terhadap hasil kali konsentrasi reaktan yang dipangkatkan koefisiennya.
Kc = [Produk]koefisien / [Reaktan]koefisien
Kesetimbangan homogen terjadi jika fase reaktan dan produk yang terlibat dalam reaksi wujudnya sama, yaitu gas (g) seluruhnya atau larutan (aq) seluruhnya.
Contoh: aA (g) + bB(g) ↔ cC (g) + dD (g)
Kc = [C]c [D]d / [A]a [B]b
Kesetimbangan heterogen terjadi jika fase reaktan dan produk yang terlibat dalam reaksi wujudnya berbeda.
Contoh: aA (aq) + bB (s) ↔ cC (s) + dD (g)
Kc = [D]d / [A]a
Pada kesetimbangan heterogen, zat yang memengaruhi tetapan kesetimbangan konsentrasi hanya yang berwujud gas (g) dan larutan (aq). Sedangkan untuk wujud padat (s) dan cairan (l) tidak termasuk di dalamnya.
Pada kesetimbangan tekanan parsial, hanya zat dengan fase gas (g) yang memengaruhi tetapan kesetimbangannya. Zat yang terlibat masing-masing akan memiliki harga tekanan parsial (P) yang menentukan harga Kp. Untuk menentukan tekanan parsial suatu zat dari tekanan parsial totalnya, maka dapat digunakan persamaan:
Px = (molx / moltotal) × Ptotal
Harga Kp ditentukan berdasarkan perbandingan hasil kali tekanan parsial produk yang dipangkatkan koefisiennya terhadap hasil kali tekanan parsial reaktan yang dipangkatkan koefisiennya:
Kp = (Pprodukkoefisien) / (Preaktankoefisien)
Contoh tetapan kesetimbangan tekanan parsial dengan zat-zat yang fasenya sama adalah sebagai berikut:

Contoh tetapan kesetimbangan tekanan parsial dengan zat-zat yang fasenya berbeda adalah sebagai berikut:
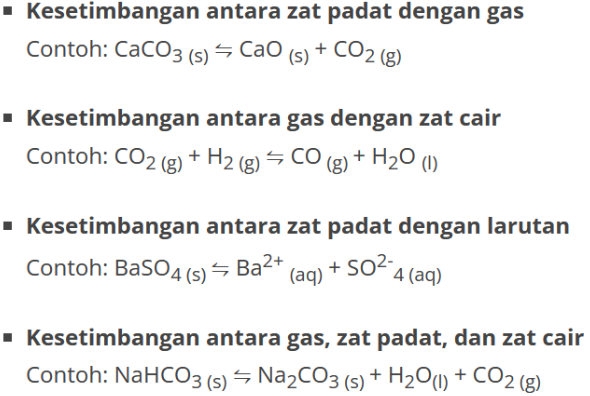
Berikut adalah penurunan rumus hubungan antara Kc dan Kp:
Jika diketahui persamaan reaksi kesetimbangan:
Rumus tetapan kesetimbangan untuk konsentrasi (Kc) dan tekanan parsial (Kp) untuk persamaan tersebut adalah:
Hubungan antara Kc dan Kp dapat dijelaskan dengan rumus berikut:
Di mana:
Konsentrasi larutan menunjukkan banyak sedikitnya jumlah molekul yang terdapat pada larutan. Semakin besar nilai konsentrasi larutan, maka jumlah molekulnya juga semakin banyak sehingga jarak antar partikelnya semakin rapat. Sebaliknya, semakin kecil nilai konsentrasi larutan, maka jumlah molekulnya juga semakin sedikit sehingga jarak antar partikelnya semakin renggang.
Konsentrasi memberikan pengaruh terhadap laju reaksi suatu reaksi kimia. Semakin besar nilai konsentrasi, semakin cepat laju reaksi. Perubahan konsentrasi juga berpengaruh pada arah pergeseran kesetimbangan.
Apabila konsentrasi pereaksi atau produk reaksi berubah, kesetimbangan akan bergeser untuk mengurangi pengaruh perubahan konsentrasi tersebut sampai tercapai kesetimbangan yang baru.
Misalnya:
aA + bB ↔ cC + dD
Penambahan konsentrasi A atau B akan meningkatkan jumlah produk reaksi. Pengurangan konsentrasi A atau B akan meningkatkan hasil reaksi atau produk.
Pengaruh tekanan berkebalikan dengan volume. Jika tekanan diperbesar, volume akan mengecil, dan kesetimbangan akan bergeser ke arah zat dengan jumlah koefisien yang lebih kecil. Sebaliknya, jika tekanan diperkecil, volume akan membesar, dan kesetimbangan akan bergeser ke arah zat yang jumlah koefisiennya lebih besar. Perubahan tekanan dan volume tidak mengubah nilai tetapan kesetimbangan (K).
2NO2 (g) ↔ N2O4 (g)
Pada sistem di atas, jika tekanan diperbesar, maka volume diperkecil dan kesetimbangan akan bergeser ke arah zat dengan jumlah koefisien yang lebih kecil, yaitu ke arah N2O4 (g). Sebaliknya, jika volume diperbesar, tekanan diperkecil dan kesetimbangan akan bergeser ke arah gas NO2 yang memiliki jumlah koefisien lebih besar.
Catatan: Jika jumlah koefisien reaktan dan produk sama, maka tidak akan terjadi pergeseran kesetimbangan.
Perubahan suhu memengaruhi kesetimbangan eksoterm dan endoterm. Kenaikan suhu mengakibatkan kesetimbangan bergeser ke arah reaksi endoterm, sementara penurunan suhu mengakibatkan kesetimbangan bergeser ke arah reaksi eksoterm. Perubahan suhu juga memengaruhi nilai tetapan kesetimbangan (K).
2SO2 (g) + O2 (g) ↔ 2SO3 (g) + kalor
Reaksi kesetimbangan di atas adalah reaksi pembentukan SO3, yang merupakan reaksi eksoterm. Jika suhu dinaikkan, sistem akan menyerap panas dan kesetimbangan akan bergeser ke arah reaksi endoterm (ke arah reaktan). Sebaliknya, jika suhu diturunkan, kesetimbangan akan bergeser ke arah eksoterm (ke arah produk).
Pada suhu tertentu, terdapat reaksi setimbang:
2SO3 (g) ↔ 2SO2 (g) + O2 (g)
Jika pada keadaan setimbang terdapat 0,04 M SO3, 0,02 M SO2, dan 0,01 M O2, tentukanlah nilai Kc!
Kc = ([SO2]2[O2]) / ([SO3]2)
Kc = ([0,02]2 × [0,01]) / ([0,04]2)
Kc = 25 × 10-3
Selesaikan pretest ini terlebih dahulu sebelum melanjutkan ke post-test.

Selesaikan post-test ini setelah Anda melakukan eksperimen di laboratorium virtual. Tes ini bertujuan untuk mengevaluasi pemahaman Anda tentang konsep kesetimbangan kimia dan aplikasi praktisnya. Jawablah dengan teliti untuk mengukur seberapa baik Anda menguasai materi yang telah dipelajari.